2021/8/18 14:00 中央流行疫情指揮中心嚴重特殊傳染性肺炎記者會
24小時最熱
【即時字幕】2021/8/18 14:00 中央流行疫情指揮中心嚴重特殊傳染性肺炎記者會
影片來源:衛生福利部疾病管制署YouTube頻道
中央流行疫情指揮中心今(18)日公布國內新增11例COVID-19確定病例,分別為6例本土及5例境外移入;另確診個案中無新增死亡。
指揮中心表示,今日新增之6例本土病例(均非居家隔離期間陽性者),為2例男性、4例女性,年齡介於20多歲至80多歲,其中1例8月14日發病,餘均為無症狀感染,個案分布為臺北市4例、新北市2例;其中2例為已知感染源、4例關聯不明,將持續進行疫情調查,以釐清感染源。
指揮中心指出,近期確診個案解隔離情形,5月11日至8月16日累計公布14,663位確診個案中,已有13,214人解除隔離,解隔離人數達確診人數90.1%。
指揮中心說明,今日新增5例境外移入個案,為1名男性、4名女性,年齡介於20多歲至40多歲,分別自美國(案15996、案15998)、沙烏地阿拉伯(案15997)、印度(案15999)、法國(案16000)入境,入境日介於5月17日至8月15日,均持有搭機前3日內檢驗陰性報告。
指揮中心統計,截至目前國內累計2,407,073例新型冠狀病毒肺炎相關通報(含2,389,646例排除),其中15,891例確診,分別為1,351例境外移入,14,487例本土病例,36例敦睦艦隊、2例航空器感染、1例不明及14例調查中;另累計110例移除為空號。2020年起累計821例COVID-19死亡病例,其中813例本土,個案居住縣市分布為新北市402例、臺北市313例、基隆市28例、桃園市26例、彰化縣15例、新竹縣12例、臺中市4例、苗栗縣3例、宜蘭縣及花蓮縣各2例,臺東縣、雲林縣、臺南市、南投縣、高雄市及屏東縣各1例;另8例為境外移入。
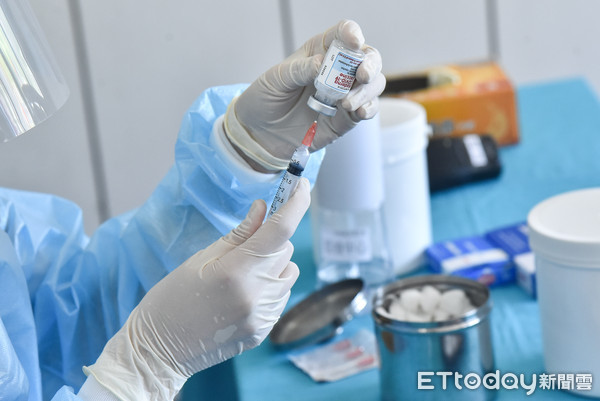
指揮中心今日並表示,「COVID-19公費疫苗預約平台」( https://1922.gov.tw/ )自8月16日10時起,已開放高端疫苗預約,至今日12時截止,總計約41.9萬人完成預約,並將於8月23日至8月29日施打。惟為利疫苗資源有效利用,將自8月18日16時至8月20日12時止,增加開放「8月13日12時以前意願登記,且為35歲至20歲(含)[即2001年8月23日(含)以前出生]民眾」預約,估計約有29.8萬人。
指揮中心說明,請符合上述預約接種資格者,可於開放預約期間進行預約,亦將於開放預約後,陸續收到提醒簡訊,請記得進行預約。此次增加開放對象同樣預定於8月23日至8月29日施打,並視疫苗供應期程調整接種場次,籲請民眾屆時準時前往接種。
指揮中心提醒,前次(8月16日10時至8月18日12時止)已宣布之符合預約資格對象,包含「65歲以上長者」、「64歲至20歲(含)第九類對象」以及「64歲至36歲(含)民眾」,依原預約時間,已於8月18日中午12時停止預約及修改;8月18日16時至8月20日12時,則僅開放上述增加開放對象進行預約。